研究支援サービス | 新着情報
- 2025/12/04
- CTCラボのインタビュー記事がバイオ・ラッド社HPに掲載されました
- 2025/10/09
- CTCラボニュース ハイブリッドE/M状態の検出例
- 2025/7/31
- CTCラボニュース 新たな展開(2025年8月より)
- 2025/5/07
- 弊社R&Dチームが流路のチャンバーをコーティングすることに成功しました。(クローズド特許)
- 2024/11/14
- 韓国 臨床統合医学癌学会 第15回秋季国際学術セミナーにおいて講演いたしました
- 2024/10/01
- バイオラッド社が米国にてマイクロ流路デバイスVer2を2024年6月にリリースしました
CTCラボニュース
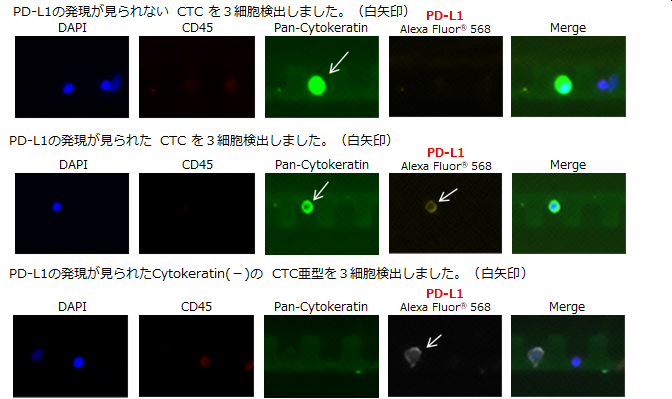
CTC(PD-L1)で見つかったCTC亜型(Cytokeratin(CK)(-), PD-L1(+))検出例
血中循環腫瘍細胞(CTC)におけるPD-L1測定は免疫療法における予後や薬剤奏功の予測・治療有効性を低侵襲的に評価することに役立つと報告されております。最近、弊社ラボでは、CTCの亜型(Cytokeratin(CK)(-), PD-L1(+))の検出例が多くなってきております。 今回はその症例の一部をご紹介するとともに、参考論文を以下に示しました。
<参考論文>
◇ Daniel J. Boffa, et al. Cellular Expression of PD-L1 in the Peripheral Blood of Lung Cancer Patients is Associated with Worse Survival, Cancer Epidemiol Biomarkers Prev. 2017 Jul; 26(7): 1139–1145.
◇ Dorothea Sonja Schott, et al. Sensitive detection of PD-L1 expression on circulating epithelial tumor cells (CETCs) could be a potential biomarker to select patients for treatment with PD-1/PD-L1 inhibitors in early and metastatic solid tumors, Oncotarget. 2017 Sep 22; 8(42): 72755–72772.
◇ Manjima Dhar, et al. Evaluation of PD-L1 expression on vortex-isolated circulating tumor cells in metastatic lung cancer, Scientific Reports. 2018; 8: 2592.
PD-L1とは

通常の体内免疫機構には、がん細胞を異物や病原体と同様に非自己物質として認識して攻撃する働きがあります。一方、攻撃する側の免疫細胞であるT細胞は、免疫応答制御のためにPD-1と呼ばれる免疫抑制受容体を持っていて、そのリガンドであるPD-L1 (programmed cell death-ligand 1) が免疫細胞のPD-1受容体に結合するとT細胞の攻撃性が抑制されます。通常であれば、この機構は過剰な免疫応答による自己免疫疾患などに陥らないためのチェックポイントとして機能します。しかしながら、がん細胞はこのチェックポイント機能をうまく利用して、がん細胞自身の表面上にPD-L1を発現させて、T細胞からの攻撃に自らブレーキをかけることが分かっています。
子宮がん患者 静脈血
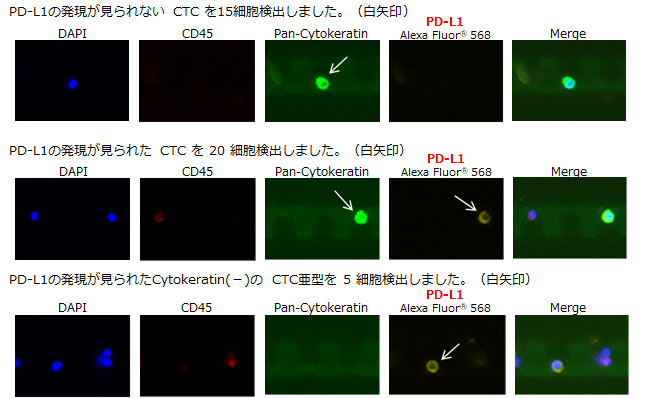

原発巣不明がん患者 静脈血
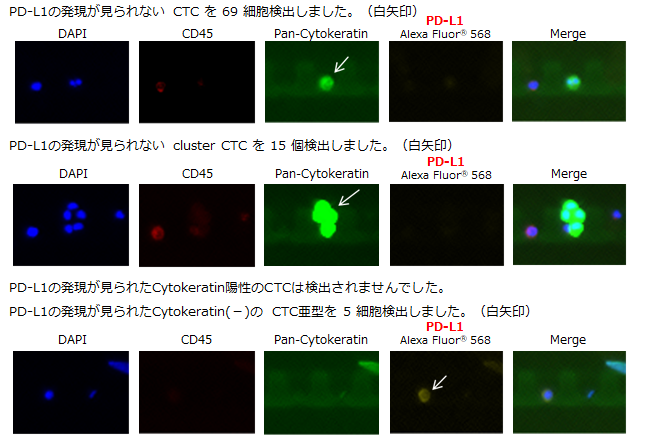

膀胱がん患者 静脈血

■News
<CTC測定に新たに3項目(PD-L1,AR-v7およびHER2)>
CTC測定 PD-L1抗体、AR-v7抗体、HER2 抗体を用いた場合の効果判定

※ AR-v7、HER2、PD-L1が陽性の場合、高陽性(High)が検出される場合があります。
検出データ例




論文紹介
【論文1】
Marius Ilie, et al. 2014, Plos One, Vol.9, Issue 10, e111597
“Sentinel” Circulating Tumor Cells Allow Early Diagnosis of Lung Cancer in Patients with Chronic Obstructive Pulmonary Disease.

CTCが検出された5人のCOPD患者はCTC検出の1~4年後にCTスキャンで肺結節が検出され、早期肺癌診断と外科的切除に至り、いずれの患者も術後12か月後のCTスキャンおよびCTCの追跡調査では腫瘍再発はなく、CTCは検出されなかったと報告されています。詳しくは論文をご参照ください。
【論文2】
Karin Ried, et al. 2017, Asian Pacific Journal of Cancer Prevention, Vol.18, 2275
Screening for Circulating Tumour Cells Allows Early Detection of Cancer and Monitoring of
Treatment Effectiveness: An Observational Study.

高リスク被験者のうち132人でCTC検出(0.2~50個CTC/mL, 平均16個/mL)され、そのうち24人(20%)で0.5~10ヶ月以内の標準スキャンにより早期癌性病変が検出されたと報告されています。
その132人中で、PSAが正常レベルでもCTCが検出された男性の50%において、PETスキャンにより早期前立腺癌が発見され、またその132人中の7人において早期の乳癌、黒色腫、卵巣癌、肺癌、腎臓癌が検出されたと報告されています。詳しくは論文を参照ください。
※1 277人のがん患者の癌種内訳

※2 がん患者におけるCTC検出数は0.2~65.4個/mLの範囲で、CTC検出数は患者のがんの状態や症状と相関があり、より高いCTC検出数に対してより進行した症例が示されたと述べられています。

※3 高リスク被験者とは、「がんの家族歴、喫煙習慣、女性における長期経口避妊薬使用またはホルモン補充療法、男性における高齢(>50歳)、その他の医療適用を有するがんのリスクが高い患者で構成される被験者」と述べられています。
CTCラボニュース 2018,12/04
2018年11月30日までの共同研究実績が1,103症例に至りました。
Stage Ⅳの3症例におけるCTC計測数の例




Microfluidic Chipによる血中循環腫瘍細胞(CTC)測定
免疫チェックポイントの検出用として抗PD-L1抗体免疫染色による共同研究を開始しております。PD-L1とは
CTCにおけるPD-L1の検出論文:[Scientific Reports (2018) 8,:2592][1]によると著者等は、免疫チェックポイント機能を阻害する抗体製剤であるPD-1およびPD-L1阻害剤を用いた近年の臨床試験では、転移性非小細胞肺癌(NSCLC)において有望な臨床結果が確認され、腫瘍生検で高いレベルのPD-L1染色を示した患者において、この効果がより良好であったことを報告しています。このことは個人向けに最適化された治療にとって重要であることから、患者の適合基準として腫瘍におけるPD-L1の発現を利用することに関心が集まっています。
現在利用できるスクリーニングの方法は、侵襲的な腫瘍生検によるPD-L1レベルの組織学的悪性度のグレード分類です。しかしながら、生検は合併症を誘発するリスクが高く、また限られた腫瘍切片からしか採取できないことから、腫瘍の不均一性 (異種性) を全体的には反映していない可能性があることを、著者等は指摘しています。
したがって、腫瘍循環細胞 (CTC) におけるPD-L1測定は患者のスクリーニングに役立ち、播種した腫瘍部位由来のPD-L1発現を測定することにより、組織におけるPD-L1生検の結果を補うことができると述べています。またCTC測定をスクリーニングの手段とするため、著者等はCTCを純度よく単離し、PD-L1で染色する方法を開発しています。CTCのPD-L1表現をモニタリングすることは、免疫治療の効果を正確に判断する薬剤応答の新たなバイオマーカーになり得ると著者等は指摘しています。
引用文献 [1]:Manjima Dhar, et al. (2018). Evaluation of PD-L1 expression on vortex-isolated circulating tumor cells in metastatic lung cancer, Scientific Reports 8, Article number: 2592.


<ペットのCTC測定も開始いたしました。>
弊社ラボでは、これまでにペットクリニックから依頼や問い合わせが多く寄せられておりました。そのため、弊社ラボではこれまでの経験を生かし、犬、猫のCTC測定を開始いたしました。
今回、CTC検出例の一部をご紹介いたします。
▶ペットのCTC測定のご出検に関して
ペットの採血につきましては、日本べクトン・ディッキンソン株式会社のEDTA入り採血管を使用します。血液は1ml採血していただき、採血後にはゆっくりと転倒混和を10回行い、24時間以内にご提出いただきます。
※犬、猫以外の動物種につきましては、弊社ラボまでお問い合わせください。
<ペットのCTC測定の検出例> 動物種:犬
犬の種類:ダックスフンド
乳がん疑い 1ml 静脈血
CTCを3細胞検出した。(白矢印) 抗体はDogに特異性のある抗体を使用

■News
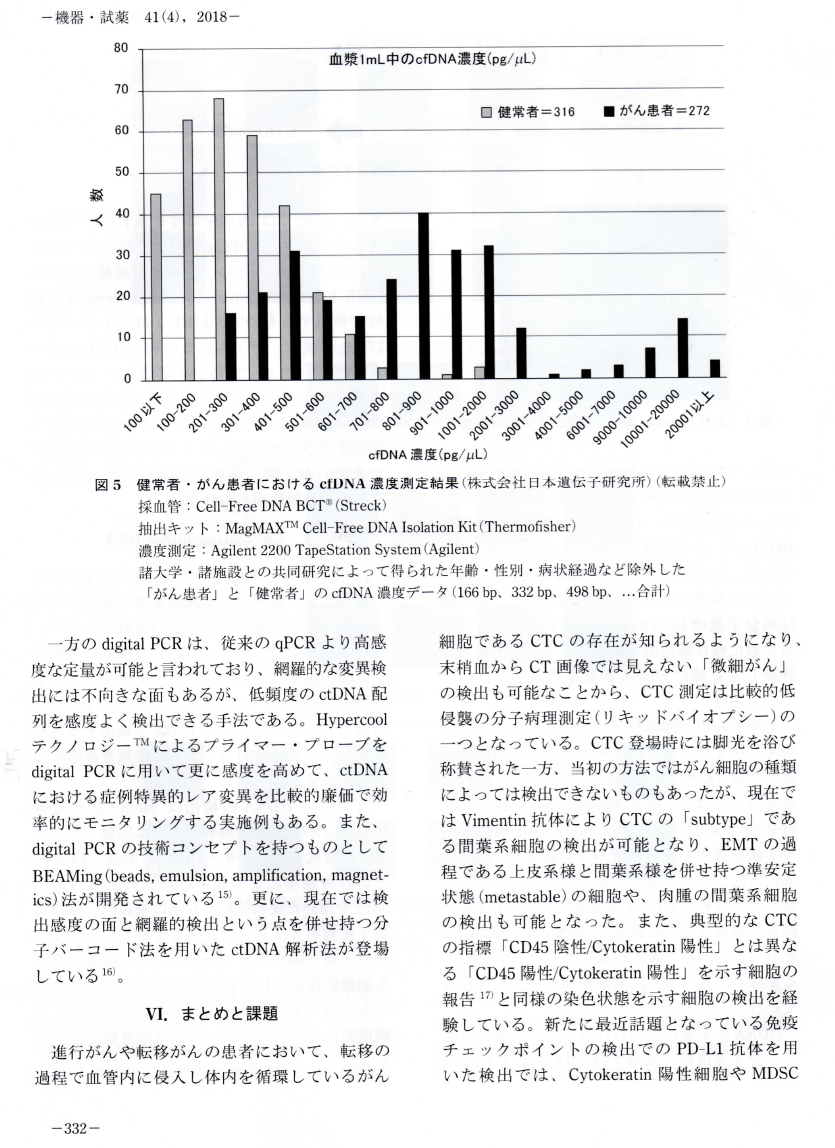
掲載誌: 医療と検査機器・試薬掲載論文名:血中循環腫瘍細胞(CTC)測定・cfDNA濃度測定
医療と検査機器・試薬, 2018,Vol. 41, No. 4,p. 326-333.







■ CTCと派生物質
(株)日本遺伝子研究所名誉研究所長 粕谷厚生(東北大学名誉教授)まえおき
ガンの診断や治療と深く関わる末梢血循環腫瘍細胞(Peripheral Blood Circulating Tumor Cell; CTC)と言う用語が研究論文はもとより、新聞でも時折見受けられるようになりました。原発巣或いは転移した腫瘍組織から遊離して血管に流れ込んだ細胞で、ガンの初期では1 mlの血液中に数個とごく微量ながら血流に乗って遠方の組織にまで浸潤し、増加しながらガンの転移や進行に支配的な役割を演じていると指摘されています。 しかもCTCは遊離後も形態や性状を多様に変化させながら体内を巡るので単に個数を計ることに留まらず、刻々と変化して行く全体の様子をも捉えることによってガンの現状や進行状況を的確に把握し、高度な治療に役立てることが期待されます。測定は末梢血を採取するだけの非侵襲的な液体生検(liquid biopsy)になりますので、簡便なところが大きな利点です。
CTCは百年以上も前に900体を超える解剖の精査などに基づき提唱されました。以来弛まぬ研究が続き、ここ20年ほどにはナノテクノロジーによる材料、加工、計測技術が進歩し、磁性微粒子、微小流路、顕微分光などを活用した血液の高感度精密測定が可能になったことで、存在が漸く実証されました。
現在では様々な分析装置が考案され、採取された血液中から定められた判定規準に従ってCTCを選んで数え上げ、ガン患者の生存率(Overall Survival; OS)や無憎悪生存率(Progression Free Survival; PFS)と対応させた分析結果が多数報告されています。
僅かですが末梢血から分離された濃縮物を観察すると、形の整ったもともとのintactなCTC (iCTC)や循環腫瘍幹細胞(Circulating Stem Cell; CSC)と言われる細胞が先ずありますが均一ではなく(heterogeneity)、上皮間葉転換(Epithelial-Mesenchymal Transition; EMT)などに由来する亜形(CTC subtype)も多数見受けられます。また細胞が幾つか集まった塊(CTC cluster, Circulating Tumor Microemboli; CTM)や、個々の死滅 (apoptosis CTC; aCTC, Necrosis) 或いは損傷、分解により生ずる破片(Granular CTC, Tumor Cell Fragment; TCF)、粒(Tumor Micro-Particle; TMP) やDNAの断片 (循環腫瘍DNA、circulating tumor DNA; ctDNA, cell free DNA; cfDNA)、も大量に見つかっています。そのほとんどがガン細胞から派生した物質でありOSやPFSとに強い相関を示す測定結果が得られています。
これらCTCは基よりガン細胞から多岐に派生して行く物質を全体的に眺めていると、ガンの転移に関わる様々な過程の端々が物質それぞれに見え隠れしているような気がして来ます。このような多様な変化を個人毎に捉えれば、症状に合わせた具体的な診断や治療に役立てることが可能になると考えます。となれば、もともとのCTCのみを計測対象とするこれまでの分析は“木を見て森を見ず”の感があります。またCTCが希有であることを考えると、測定対象を広げることによって検出の取りこぼしや見誤りを防ぎ、測定量も増えて精度や信頼性の大幅な向上にも繋がり非常に有利になります。
実際に測定対象をCTCに限らず、ガン細胞から派生する物質を広く含めた分析例について幾つか論文紹介します。それぞれ測定対象と結果を抜き出して部分的に概訳してありますので、詳しくは原著を参照下さい。
「CTCと派生物質」はこちら
■News
CTCラボニュース 2018,7/27当CTCラボの微小流路デバイス法は、CTCと白血球の変形特性が大きく異なることに基づき原発巣から漏れ出たCTC(Type.1)と、EMT(転移能を獲得した悪性の腫瘍細胞)の可能性があるCTC(Type.2)を測定するものです。「血液の固定処理をしなかった」場合、癌細胞の中には7.5µmから8µmのPore channel(細い孔)をすり抜けてしまう細胞があるという理由により、血液の固定処理を行うことにしています。特にmessenchymal like cellのような線維芽細胞様の形態の細胞のほとんどが、5µmのpore channelでも簡単にすり抜けてしまうことがわかりました。
図1:Pore channelをすり抜けたMessenchymal like cellのcluster
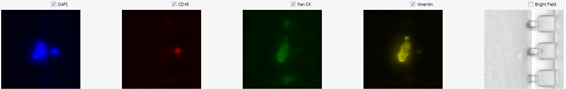

当初は走査型電子顕微鏡でCTCを見ながら、この細胞の触手を固定できないか?さらには細胞の形態を損なわない固定処理はないか?と思い巡し、開発を始めました。試行錯誤を繰り返して得られた実験結果から、現在は定められた固定液、濃度、時間によって厳密に固定処理を行っております。Micro流路chipの長所は、3Dであることにより、CTCのviabilityの強弱が明瞭に観察できることです。逆に細胞内の観察においては、2D解析よりも劣るという欠点もあり、稀に核が検出されにくい場合もあります。癌細胞を風船に例えるとしましょう。膨らませたばかりの風船は「みずみずしい、張りのある、正にviabilityの高い(強い)Intactな細胞」を表現していると思います。時間が経つにつれ、風船は徐々にしぼんでいきます。しぼんだ風船になぞらえて、私たちはこの状態をviabilityの低い(弱い)細胞と表現しております。実際に多くの癌患者様の治療後のCTCは、Viabilityが低い状態であり、intactな細胞から徐々にintactではない細胞へと変化していくのが見られます。逆に、viabilityが低い細胞から急にViabilityの高い細胞へと変貌した姿に遭遇する場合もあります。さらには、終始一貫してviabilityの変わらない細胞もあります。それはmetastable cell(Cytokeratin陽性とVimentin陽性のハイブリットタイプ:転移の準備段階の細胞と思われている)やmessenchymal like cell(間葉系細胞で線維芽様の形態を見せる)です。これらの細胞は常にViabilityが高く(強く)、共同研究による実験数は10例程で未だ少ないのですが、Pore channelで捕捉し回収した細胞を培養したところ、その増殖力には凄まじいものを感じております。このたび、共同研究に参加いただいた多くの先生方のご支援により、一つの節目となる1000件に到達することができました。当研究室では、さらに一層の開発を進めておりますので、その一部をお伝えいたします。すでに第3次共同研究募集により、PD-L1抗体を用いたCTC測定が始まっております。またCTC測定において、CD45が非常に強く発現しているMDSCと思われる細胞が偶然に検出されたため、MDSC測定の準備も進めております。
図2:一般的に見られるCD45強陽性のリンパ球


図3:上記リンパ球の10倍以上の蛍光強度を示す細胞(MDSCが疑われる細胞)


CTCラボニュース 2017,10/20
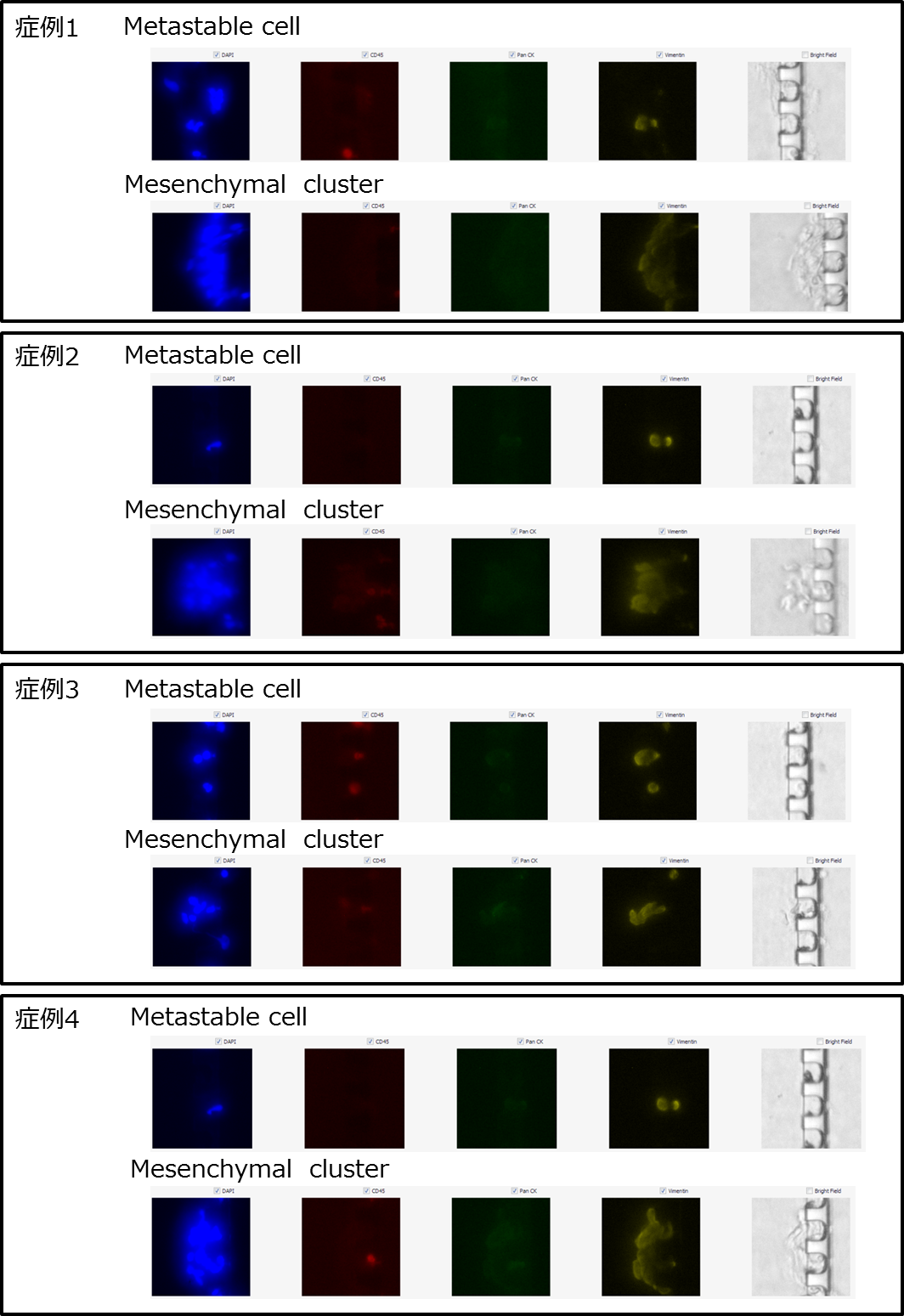
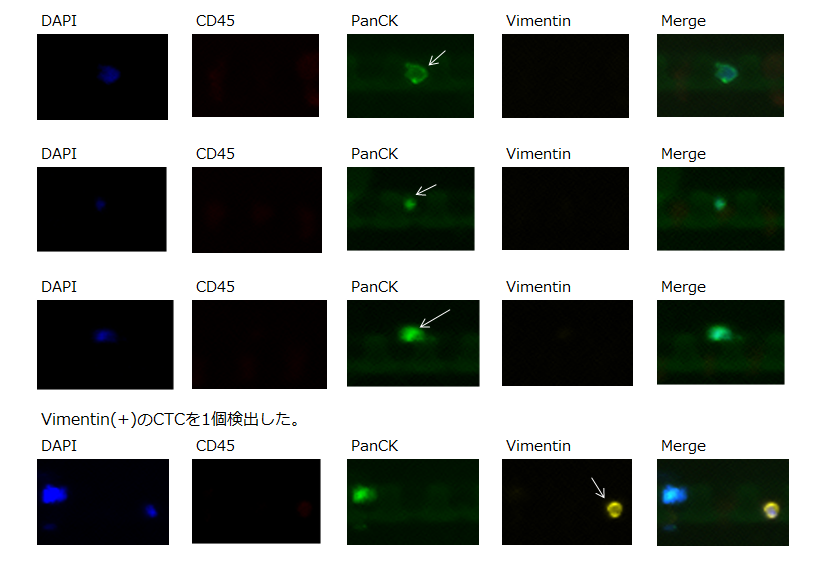
上皮-間葉移行(Epithelial-to-Mesenchymal Transition 「EMT」)とphenotype
上皮様(epithelial)から転移可能もしくは準安定(metastable)細胞を経て間葉系(mesenchymal)の細胞へ変化しています。